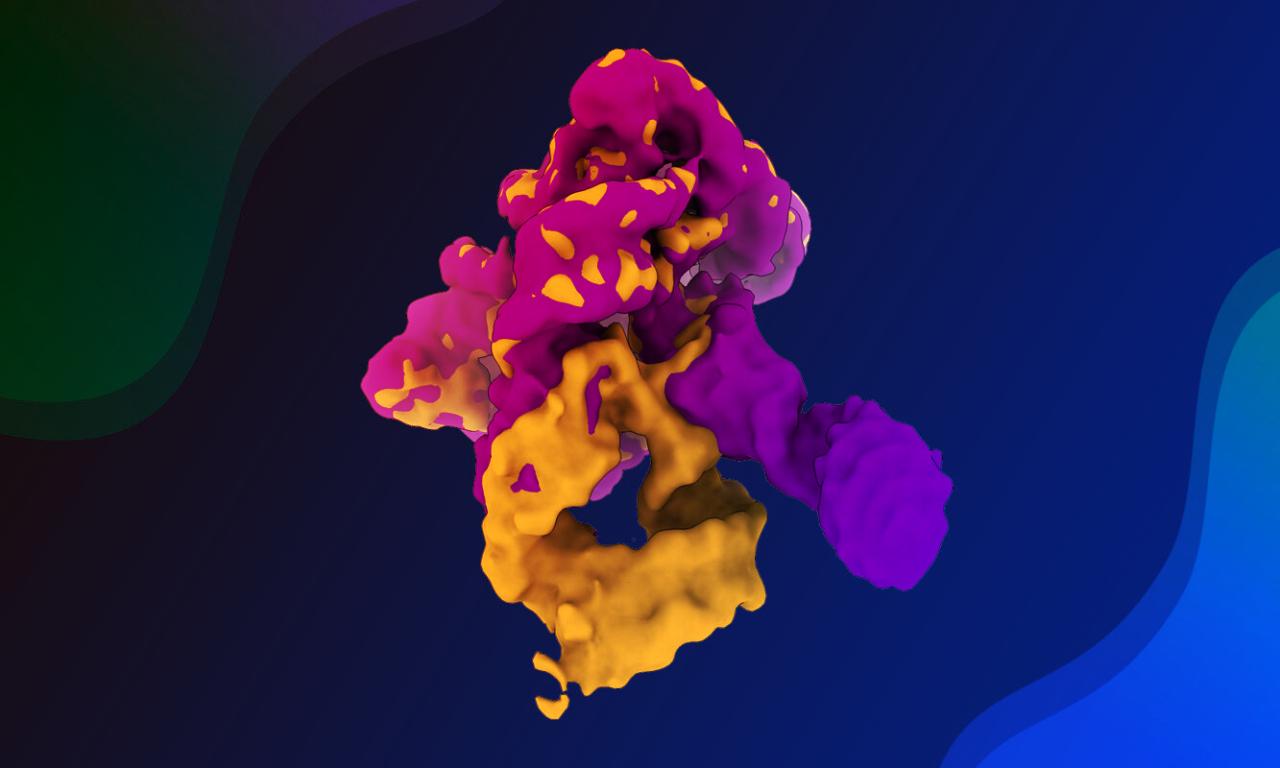
Úttörő megfigyelés: az önmetsző ribozim szerelése
A Marcia-csoport a Nature Communications-ben közölt kutatásában korszerű szerkezeti biológiai technikákat kombinált. Ezek között szerepelt a krio-elektronmikroszkópia (cryo-EM), kis szögű röntgenszórás (SAXS), RNS-kémiai és enzimológiai vizsgálatok, képfeldolgozás és molekuladinamikai szimulációk. Így figyelték meg, ahogy egy önmetsző ribozim, vagyis egy saját “vágásra és ragasztásra” képes RNS pontos szerkezetté áll össze. Az Uppsala Egyetem és az EMBL Grenoble szakértői a legmodernebb eszközparkot és nemzetközi együttműködéseket használták a sikerhez.
Külön figyelmet érdemel, hogy a kutatócsoport kifejezetten ehhez a projekthez tervezett egyedi cryo-EM képfeldolgozási stratégiákat, amelyeket Hamburgban, a CSSB-ben dolgoztak ki, valamint az Istituto Italiano di Tecnologia is fejlett molekuladinamikai szimulációkkal járult hozzá.
Az RNS: nehezen szelídíthető, mégis feltárható
Az RNS szerkezetének feltérképezése komoly kihívás, hiszen rendkívül rugalmas és negatív töltésű, emiatt a leképezése rendkívül nehéz. Hosszú hónapok aprólékos mikroszkópos vizsgálata és válogatása kellett ahhoz, hogy végül valóban mozgásban láthassák ezt a molekulát. Ezzel a módszerrel a kutatók most először “forgathatták le”, hogyan kerüli el a ribozim a működésképtelen, hibás szerkezetű állapotokat, vagyis a biológiai “bakikat”, és rendeződik katalitikus, működőképes formává.
Domain 1: az RNS rendezője
A sikeres “előadás” kulcsa az úgynevezett Domain 1 (D1), vagyis a ribozim központi váza, amely egyfajta molekuláris kapuként irányítja a további domének (D2, D3, D4) csatlakozását. A D1 finom mozdulatai pontosan jelzik, mikor léphet be a következő domén a szerkezetbe. Csak akkor kapcsolódik be a következő rész, amikor minden megelőző elem helyesen összeállt, így hibátlanul jut el a molekula a végső, katalitikus konfigurációhoz, ami elengedhetetlen a ribozim működéséhez.
Rejtett pillanatok és új technológiák
A csapat százezernyi egyedi RNS-molekula elemzésével rekonstruálta a “forgatás” köztes jeleneteit, amelyek a hagyományos kristályszerkezeteken láthatatlanok voltak. Feltételezhető, hogy ezek a gyorsan váltakozó formák elengedhetetlenek a molekula szerkezetváltásához. Az újszerű cryo-EM képfeldolgozás és a SAXS-eredmények, valamint a szimulációk lehetővé tették, hogy minden szerkezeti “pillanatfelvételt” tökéletesítsenek és felépítsék a teljes történetet. Meglepő módon kiderült: minimális energia kell a szerkezeti váltáshoz, ezáltal az RNS simán vándorol egyik formából a másikba, és a folyamat számítógépesen is könnyebben modellezhető.
Ősi eszközök és modern alkalmazások
A most vizsgált II. csoportú intronok, vagyis ezek a ribozimok, az emberi RNS-szerkesztő gépezetének, a spliceoszómának az őseit képviselik. Annak feltárása, miként kerülik el a kinetikai csapdákat, nemcsak a korai, RNS-alapú élet evolúciójához ad kulcsot, hanem új irányt is mutat az RNS-tervezésben: a jövő biotechnológiája sablonként használhatja ezeket a példákat, hogy a gyógyszeriparban vagy a nanotechnológiában megfelelően hajtogatható RNS-molekulákat hozzanak létre.
Mesterséges intelligencia: új korszak kezdete az RNS-kutatásban
Az elkészült részletes adatsorok és mechanizmusok kiváló alapot kínálnak az MI-modellek tanításához. Néhány itt feltárt szerkezetet már használtak a nemzetközi CASP versenyeken, ahol a fehérjeszerkezet-előrejelzés forradalmát hozó AlphaFold is feltűnt. Összefoglalásként megjegyezhető, hogy az MI és a precíz kísérleti módszerek találkozásával új távlatok nyílnak az RNS szerkezeti biológiájában, ahol az MI, a cryo-EM és a hagyományos struktúraelemzés közösen alakítják ki az élet egyik legsokoldalúbb molekulájának jövőbeli megértését és előrejelzését.