Mitokondrium – több, mint energiaforrás
A mitokondrium a legtöbb összetett sejt nélkülözhetetlen alkotórésze, amely nem csupán energiát szolgáltat az adenozin-trifoszfát (ATP) előállítása révén, hanem saját, csak anyai ágon öröklődő genetikai anyaggal is rendelkezik. Valaha önálló, prokarióta élőlények lehettek, amelyek végül szimbiózisra léptek az evolúció hajnalán a gazdasejtekkel.
Bár régóta közismert, hogy a mitokondriumok a sejtek energiaellátásáért felelősek, egyre több kutatás mutat arra, hogy közvetlenül befolyásolják a sejtosztódást, a differenciálódást, az öregedést, a jelátvitelt és a fejlődés időzítését is. Ezeket a funkciókat részben a sejtmag DNS-ével való „párbeszéden”, azaz crosstalkon keresztül végzik, ám ennek részletei eddig rejtve maradtak.
Mesterséges mitofágia: lökd ki a mitokondriumokat!
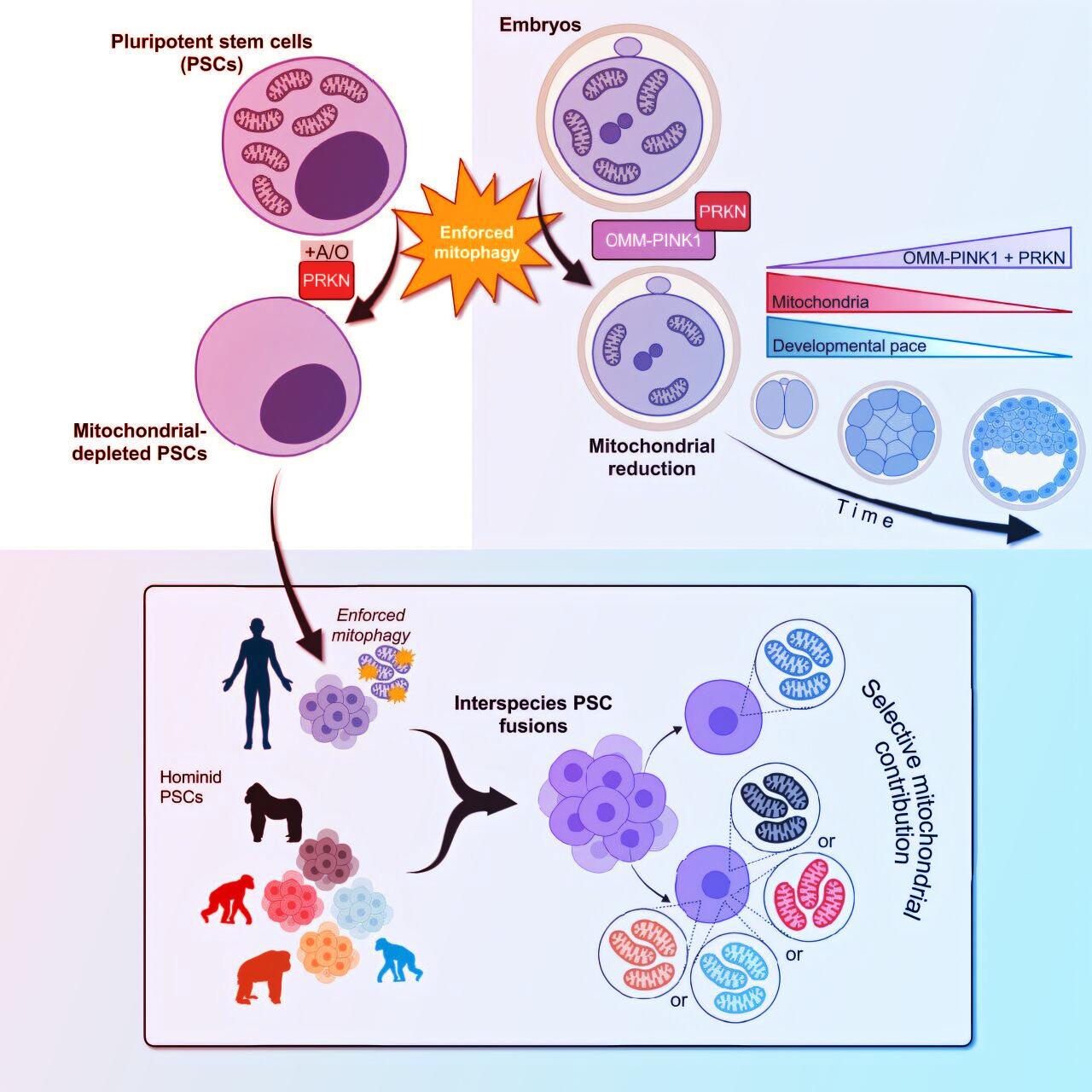
A kutatók egy, a mitofágiának nevezett, természetes sejtes folyamatot vettek alapul, amely során a sejt lebontja elöregedett vagy sérült mitokondriumait. Ezt a folyamatot géntechnológiával felerősítették, így a sejtek minden mitokondriumuktól megszabadultak. A kísérletekben laboratóriumban növesztett humán pluripotens őssejtekkel (hPSC), valamint egér őssejtekkel dolgoztak.
Ez a drasztikus beavatkozás ugyan megállította a sejtosztódást, de meglepő módon a sejtek akár öt napig is életképesek maradtak – még akkor is, ha káros mitokondriális DNS-t hordoztak. Ez azt sugallja, hogy az eljárás széles körben alkalmazható különféle sejttípusokon és fajokon, továbbá hasznos eszközzé válhat az alapkutatásban és a gyógyászatban is.
Cserélhetők-e a mitokondriumok fajok között?
A tudósok következő lépésként összeolvasztották a humán őssejteket emberszabású majmok (csimpánz, bonobó, gorilla, orángután) pluripotens őssejtjeivel, így létrehozva “kompozit” sejteket, amelyek két különböző eredetű sejtmagot és mitokondriumokat hordoztak. Megdöbbentő eredmény: ezek a sejtek automatikusan kiszűrték a majom-mitokondriumokat, kizárólag az emberi változatot hagyva meg.
Egy újabb, ellenkező irányú kísérletben előbb eltávolították az emberi mitokondriumokat, majd összeolvasztották a sejteket majomtól származóakkal – így csak nem emberi mitokondriumok maradtak. Az elemzések szerint a több millió évnyi evolúciós távolság ellenére a mitokondriumok nagyjából felcserélhetők, és csak elhanyagolható különbségeket okoztak a génaktivitásban.
Érdekes módon a génaktiválódás eltérései főként az agyfejlődéssel és neurológiai betegségekkel voltak kapcsolatban. Ez arra utal, hogy a mitokondriumok is szerepet játszhatnak az ember és közeli rokonai agyi eltéréseiben, bár további kutatások, például ilyen kompozit sejtekből származó idegsejtek összehasonlítása szükséges.
Mitokondriumok nélkül a fejlődés sem a régi
A módszert egér embriókon is kipróbálták: azok az embriók, amelyekből a mitokondriumok több mint 65%-a hiányzott, nem tudtak beágyazódni az anyaméhben. Azoknál, ahol csak a mitokondriumok harmada tűnt el, a fejlődés lelassult ugyan, de 12,5 napos fejlődés után helyreállították eredeti mitokondriumszintjüket és behozták a lemaradást.
Új korszak kezdete a sejtbiológiában
Az új genetikai eszköz, amellyel kényszerített mitofágiát lehet előidézni, eddig soha nem látott részletességgel mutatja meg, milyen széles körű és meglepő szerepet tölt be a mitokondrium a sejtek, szervek, fejlődés, öregedés és akár a fajok evolúciója szempontjából. Az MI-vezérelt mitofágia hamarosan alapja lehet a mitokondriális betegségek új terápiáinak és az alapkutatásoknak egyaránt.