Az utolsó csomagolási trükk nyomában
Sokáig rejtély volt, miként éri el a kromatin ezt az extrém szintű tömörödést. 2019-ben azonban Michael Rosen és csapata laboratóriumi körülmények között azt találta, hogy a nukleoszómák természetesen gyűlnek össze membrán nélküli cseppekbe, az úgynevezett kondenzátumokba. Ez a folyamat nagyon hasonlít arra, ahogyan az olajcseppek válnak le a vízből – a jelenséget fázisszétválásnak nevezik, és nagy valószínűséggel az élő sejtekben is ezt a mechanizmust használja a kromatin.
Ezek a kondenzátumok több százezer, gyorsan mozgó molekulából épülnek fel. Együttműködésük révén olyan tulajdonságokat mutatnak, amilyenek külön-külön egyetlen molekulánál sem jelennek meg. E csoportos tulajdonságok határozzák meg, hogyan alakulnak ki a kondenzátumok, és hogyan őrzik meg tulajdonságaikat.
Példátlan részletességű felvételek
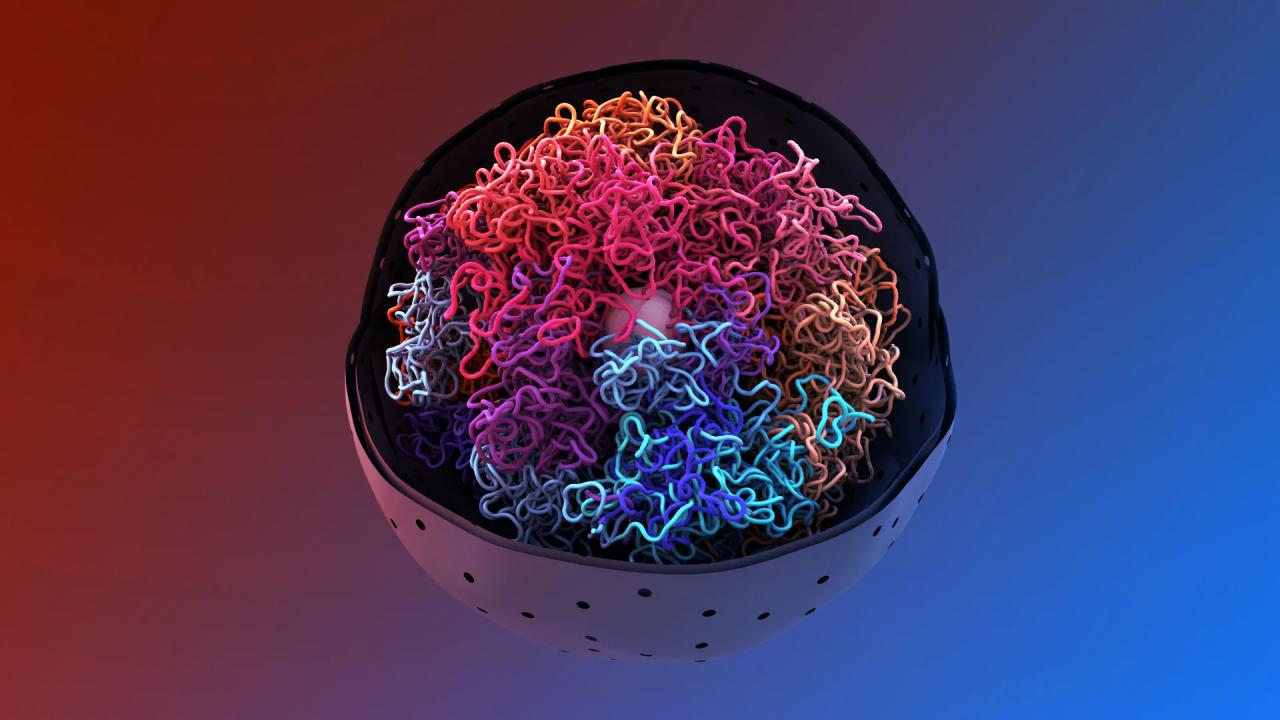
A Rosen-csoport nemzetközi kutatókkal együttműködve új, nagyfelbontású képalkotó módszerekkel most minden korábbinál részletesebben tudta feltérképezni a mesterséges kromatin-kondenzátumok belső felépítését. Ezek a felvételek pontosan bemutatják, miként csomagolódnak be a kromatinrostok és nukleoszómák a csepp alakú struktúrákba, sőt, hasonló módszerekkel már élő sejtekben is vizsgálták a kromatint.
Számítógépes modellek és fénymikroszkópos vizsgálatok segítségével sikerült megérteni, hogy a nukleoszómák közötti úgynevezett linker DNS hossza döntően befolyásolja a teljes struktúra elrendeződését. Ez megmagyarázza, miért megy végbe könnyebben a fázisszétválás bizonyos kromatinrostoknál, és miért különböznek anyagi tulajdonságaik, ha más-más típusú kromatinból épülnek fel.
Tágabb távlatok: betegségek és terápiák
A felfedezés messze túlmutat a kromatin világán: új modellt kínál minden olyan biomolekuláris kondenzátum vizsgálatára, amelyek sejten belül kulcsfontosságú feladatokat látnak el a génszabályozástól a stresszválaszokig. Mindez különösen jelentős, mert az eredmények rávilágítanak arra, hogy ha a kondenzáció folyamata sérül, az súlyos betegségekhez – így neurodegeneratív kórokhoz vagy daganatokhoz – vezethet. Most először válik lehetővé, hogy a molekulák szerkezetét összekapcsoljuk a kondenzátumok nagyléptékű tulajdonságaival, ami új terápiás utakat nyithat meg a jövőben.