Újabb veszély: az antibiotikum-rezisztencia árnyéka
Az elmúlt években világszerte egyre súlyosabb lett a helyzet: a baktériumok hihetetlen gyorsasággal válnak ellenállóvá a jelenlegi gyógyszerekkel szemben. Bár Magyarországon nem minden adat naprakész, az USA-ban már minden évben tízezrek halnak bele olyan fertőzésekbe, amelyek egyetlen elérhető antibiotikumra sem reagálnak – és ez a szám folyamatosan nő. A kutatók kénytelenek teljesen új támadási pontokat keresni ezek ellen a kórokozók ellen, mert az eddig bevált gyógyszerek hatékonysága rohamosan csökken.
A bakteriális sejtfal – egy régi-új célpont
A bakteriális sejtfalat alkotó peptidoglikán (egy szinte páncélként működő réteg) szintézise régóta célpontja az antibiotikum-fejlesztésnek. A folyamat bakteriális sajátosság, az emberi szervezet nem rendelkezik ilyen struktúrával, ezért ideális célpont. A penicillin vagy az amoxicillin például épp ezt a peptidoglikán-szintézist gátolja – ám sajnos a baktériumok már ezeket is kijátsszák.
A MurJ fehérje: a bakteriális gyenge pont
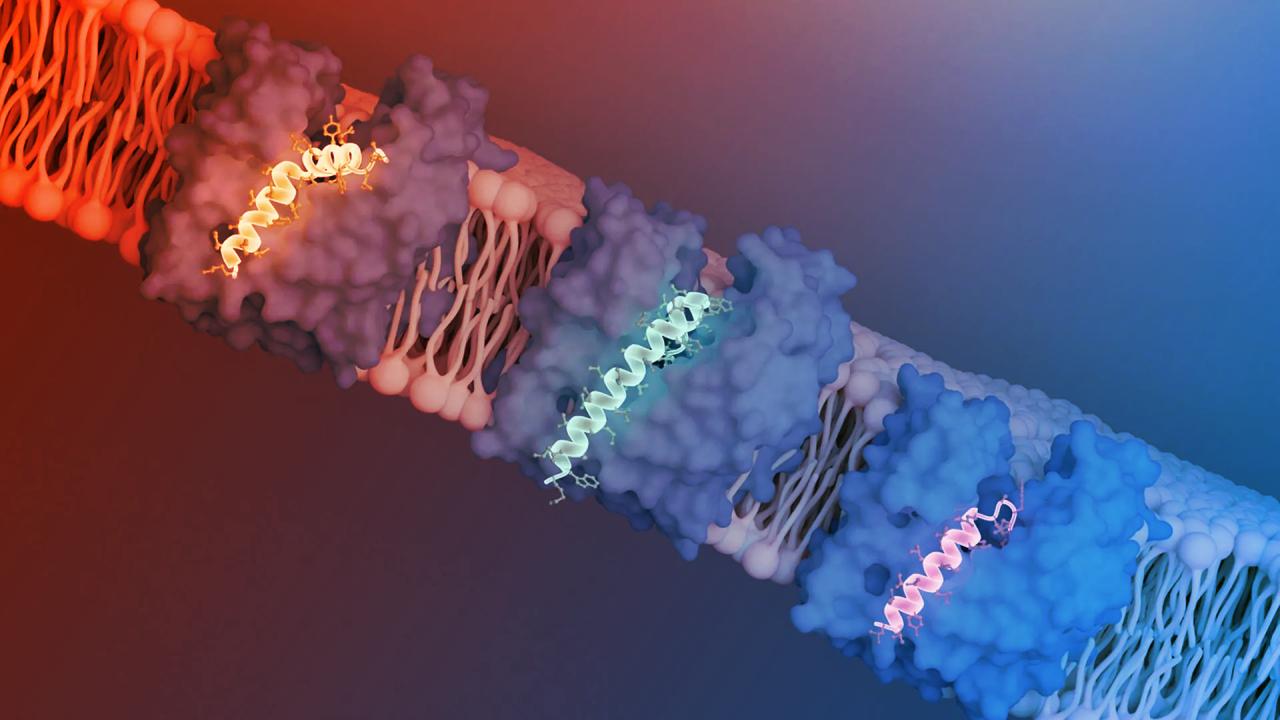
Három kulcsfontosságú fehérje (MraY, MurG és MurJ) vezérlik a peptidoglikán alkotóelemeinek szállítását a bakteriális belső membránon át. Ha bármelyik működése megszakad, a baktérium sejtfala nem épül meg, és a sejt elpusztul. E fehérjék szerepe régóta ismert, de jelenleg még nincs humán használatú gyógyszer, amely közvetlenül ezeket támadná. Úgy tűnik azonban, hogy a természet már megtalálta a megoldást – mégpedig a fágok révén.
Hogyan trükköznek a baktériumokat fertőző fágok?
A történet másik oldala, hogy a kis DNS- vagy RNS-alapú fágok behatolnak a baktériumba, majd ki is kell törniük onnan; ehhez át kell rágniuk magukat a peptidoglikán rétegen. Ezek a fágok egyszerű, de rendkívül hatékony „egygénes lízisfehérjéket” (ún. Sgl-fehérjéket) termelnek, amelyek közül több is a MurJ-t blokkolja.
A MurJ egy „flippáz”, azaz képes az előanyagokat átbillenteni a membrán egyik oldaláról a másikra. A kutatók kriogén elektronmikroszkóppal vizsgálták, miként tapadnak rá ezek a speciális vírusfehérjék (például az SglM, az SglPP7 és újoncként az SglCJ3). Mindegyik ugyanazt teszi: rögzíti a MurJ-t kifelé néző állapotban, így az nem tud többé anyagokat átbillenteni, a sejtfalépítés leáll, a baktérium elpusztul.
A természet ötlete inspirálhatja az új gyógyszereket
A kutatók számára különösen meglepő volt, hogy egymástól teljesen eltérő fehérjék, különböző fágokban, szinte azonos taktikát alkalmaznak: mind ugyanazt a bakteriális gyenge pontot támadják. Ez tipikus példája a konvergens evolúciónak. A következtetés egyértelmű: a MurJ a baktériumok Achilles-sarka lehet, amelynek blokkolása hatékony baktériumölő stratégiát jelenthet. Ráadásul, mivel a MurJ kifelé néző szerkezete hozzáférhetőbb, gyógyszerfejlesztéshez is ideális kiindulópont.
Egy új fejezet nyílhat az antibiotikumok történetében
A most leírt, Jones-féle SglCJ3 is pontosan ugyanabban a pozícióban rögzíti a MurJ-t, mint az eddig vizsgált Sgl-ek. Ezzel a kutatók alátámasztották, hogy a fágok természetes úton találtak rá a szuperbaktériumok kiiktatásának receptjére. A jövőben várható, hogy további fágokból izgalmas új fehérjéket szűrnek ki, amelyek egyre hatékonyabbá tehetik az antibiotikum-fejlesztést. A felfedezés bizonyítja: a természet kreativitása orvosi innovációhoz vezethet, ha sikerül követni az evolúció példáját.